
Когда в организме появляется бактерия или вирус, перед встаёт сложная задача: нужно создать антитела-иммуноглобулины, которые связывали бы вторгшийся патоген с максимальной эффективностью. Проблема в том, что вирусов и бактерий — огромное количество, вирусных и бактериальных белков — тоже, а потому получается, что В-клетки должны уметь производить абсолютно любой иммуноглобулин, чтобы схватить патоген за его белок и натравить на него иммунные клетки.
С разнообразием антител у В-клеток проблем нет — благодаря , сложному молекулярно-генетическому процессу, позволяющему монтировать колоссальное число генов для синтеза иммуноглобулинов. Но обычно в организме присутствует сразу много В-клеток, синтезирующих свои антитела. И при возникновении инфекции из разнообразия уже имеющихся антител нужно отобрать какие-то одни — самые эффективные — и не тратить ресурсы на синтез других. Для объяснения того, как это происходит, была выдвинута , но и она описывала отбор нужных В-клеток лишь в общих чертах.
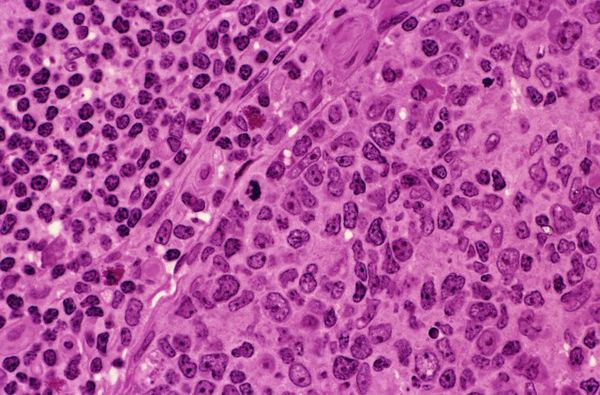
| Срез чрез зародышевый центр (слева) лимфатического узла (фото ). |
Группе исследователей под руководством Кай-Майкла Тёльнера из (Великобритания) и Михаэля Мейер-Хермана, представляющего (Германия), удалось объяснить этот процесс более детально. По их словам, при отборе нужных В-клеток работают те же механизмы, что действуют в эволюции. Созревание и подгонка В-клеток происходят в специальных зародышевых центрах лимфатических узлов. На поверхности каждого В-лимфоцита есть связывающие рецепторы, которые обладают той же специфичностью, что и выделяемые клеткой антитела. Иными словами, и мембранный белок, и секретируемый иммуноглобулин у одного и того же В-лимфоцита связывают одну и ту же вражескую молекулу, делая это с одинаковой эффективностью.
Так вот, как пишут исследователи в , в зародышевых центрах есть не только антитела, которые синтезируют созревающие там В-клетки: туда заходят ещё и другие иммуноглобулины, синтезированные другими линиями клеток и уже до инфекции присутствовавшие в организме. И сюда же заглядывают частицы антигена — вирусные и бактериальные белки, сами бактерии и т. д. В результате в центрах созревания В-клеток разворачивается конкурентная борьба между клетками и чужими антителами за то, кто сильнее свяжет антиген. Если клетка связала вирусную или бактериальную молекулу прочнее, чем чужой иммуноглобулин, она получает шанс: в клетку с мембраны уходит «сигнал выживания», который поощряет её работать над синтезом собственных антител. Если же клетка связала антиген плохо, она отправляется «в расход» — в точности так, как это происходит с видом-неудачником во время естественного отбора. В данном случае силой естественного отбора служит инфекция, а соревнование идёт между клетками и антителами.
Результаты исследований были подтверждены как в теоретической математической модели молекулярно-клеточного отбора, так и в опытах на мышах. Очевидно, эти данные могут оказать самое непосредственное влияние на разработку вакцин: например, можно было бы придумать, как с помощью искусственных, вводимых извне антител поощрить собственные В-клетки организма производить более эффективные иммуноглобулины для борьбы с инфекцией.
Введите слово или фразу для поиска: (например, «профендер»)
